 Responsable : Jean-Yves Hogrel
Responsable : Jean-Yves Hogrel
Objectifs
Au sein du Centre d’Exploration et d’Évaluation Neuromusculaire (CEEN) de l’Institut de Myologie, l’objectif principal du laboratoire de Physiologie et d’Evaluation Neuromusculaire (NeuPEL) est de comprendre les altérations et les adaptations du système neuromusculaire et d’évaluer les effets d’interventions thérapeutiques. Le NeuPEL est un laboratoire pluridisciplinaire avec des expertises multiples dans le domaine de la physiologie, des technologies pour la santé, des sciences de la réhabilitation, et de la science des données. Dans ce cadre, nous développons des approches innovantes pour l’évaluation non-invasive du système neuromusculaire, des performances motrices, et de l’activité physique. Ces approches sont particulièrement explorées chez des patients atteints de pathologies neuromusculaires lors de protocoles de recherche clinique pour comprendre l’évolution des maladies et évaluer l’efficacité de thérapies innovantes. Ces approches sont également explorées dans d’autres situations cliniques impliquant un retentissement neuromusculaire telles que le vieillissement, les maladies chroniques, les soins intensifs, et l’exercice. Le laboratoire conduit également des essais prospectifs concernant les effets de l’activité physique et l’utilisation de dispositifs d’assistance innovants chez des patients atteints de pathologies neuromusculaires. Le NeuPel est impliqué dans le diagnostic clinique de patients présentant des maladies métaboliques rares. Enfin, le NeuPel exerce également des activités de prestations et de conseils auprès de collaborateurs académiques et industriels (aide au design, métrologie clinique, formations, évaluation de patients).
Le NeuPel est rattaché à l’école doctorale Physiologie Physiopathologie (ED394, Sorbonne université).

Membres
- Jean-Yves Hogrel, PhD, HDR, Ingénieur biomédical, Responsable du laboratoire
- Valérie Decostre, PhD, Kinésithérapeute, Chargée de recherche
- Simone Birnbaum, PhD, Kinésithérapeute, Chargée de recherche
- Erwan Gasnier, PhD, Chef de projet de recherche clinique
- Isabelle Ledoux, MSc, Ingénieur biomédical
- Audrey El Kaim, Kinésithérapeute
- Pauline Santmarty, Kinésithérapeute
- Romain Feigean, MSc, Doctorant
- Thomas Marques, Ingénieur d’études
Contact
Tel : 01 42 16 58 79
Email : eval@institut-myologie.org
Approches innovantes pour l’évaluation non-invasive du système neuromusculaire
Évaluation de dispositifs d’assistance – AssistMyo
Exercice et activité physique dans les pathologies neuromusculaires – ExMyo
Activités de diagnostic clinique
Implication dans la recherche clinique
Expertise et services
Brevets
Nos dernières publications
Approches innovantes pour l’évaluation non-invasive du système neuromusculaire
Peu de temps après la création du laboratoire, il est vite apparu que les solutions commercialisées pour l’évaluation des patients neuromusculaires présentaient des limitations rédhibitoires ou n’existait tout simplement pas. En 1999, nous avons participé à l’évaluation de l’une des premières thérapies géniques locorégionale dans la dystrophie musculaire de Duchenne (essai Transgene). Un plasmide était injecté dans le muscle extenseur radial du carpe. Il n’existait pas de dispositif permettant mesurer le couple d’extension du poignet. Nous avons alors développé un dynamomètre spécifique (MyoWrist) afin d’évaluer de façon optimale ce traitement innovant. Le nombre d’approches thérapeutiques dans les pathologies neuromusculaires a explosé ces dix dernières années. Le choix des critères de jugement (outcome measures) principaux et secondaires est crucial pour évaluer les potentiels bénéfices des traitements. Un de nos objectifs est donc de produire les connaissances permettant de choisir le meilleur critère pour évaluer le système neuromusculaire et les performances motrices dans une situation clinique donnée. Le développement de mesures non-invasives est également un des objectifs clef des programmes de recherche du laboratoire. Nos approches actuelles reposent principalement sur une combinaison de dispositifs spécifiques, de mesures inertielles, de mesures électrophysiologiques, et d’imagerie ultrasonore multiparamétrique (élastographie par onde de cisaillement, imagerie ultra-rapide). La validation des différentes approches et dispositifs que nous élaborons ainsi que le développement de données normatives est une activité et une expertise centrale du laboratoire.
Dispositifs d’évaluation de la fonction neuromusculaire – MyoTools
Les MyoTools sont un ensemble de dispositifs développés au laboratoire permettant principalement l’évaluation de la force musculaire. Ces derniers sont particulièrement adaptés à l’évaluation d’adultes et d’enfant atteints de pathologies neuromusculaires mais trouvent également de nombreuses applications dans d’autres champs cliniques (vieillissement, maladies cardio-respiratoires et métaboliques, …). Au-delà des dispositifs en eux-mêmes, les MyoTools englobent des procédures standardisées, une démarche qualité assurant la meilleure métrologie clinique possible, et une offre de formation. Les MyoTools sont actuellement utilisés dans de nombreux essais cliniques à travers le monde.
Plusieurs MyoTools sont industrialisés et distribués par nos partenaires.
MyoTools
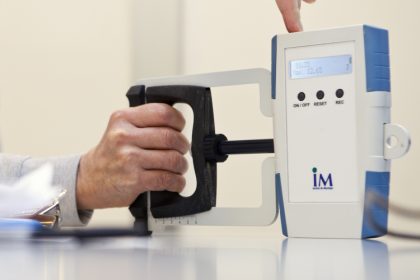
MyoGrip- Un dynamomètre de haute précision pour l’évaluation de la force de préhension (breveté)
La MyoGrip est un dynamomètre électronique spécialement conçu pour mesurer la force de préhension en condition isométrique et adapté aux patients très faibles. La MyoGrip a été développée pour répondre aux exigences d’un suivi quantifié et rigoureux de la force de préhension, notamment dans les essais thérapeutiques. La MyoGrip mesure des forces allant de 0 à 90 kg avec une résolution de 10 g et une précision de 50 g. La largeur de la poignée est réglable.
Fabriqué et distribué par les Ateliers Laumonier (contact@laumonier.fr).

 MyoPinch – Un dynamomètre de haute précision pour l’évaluation de la force de la pince pouce-index (breveté)
MyoPinch – Un dynamomètre de haute précision pour l’évaluation de la force de la pince pouce-index (breveté)
Le MyoPinch est un dynamomètre électronique spécialement conçu pour mesurer la force de pince pouce-index et adapté aux patients très faibles. Le MyoPinch a été développé pour répondre aux exigences d’un suivi quantifié et rigoureux de la force de pince pouce-index, notamment dans les essais thérapeutiques. Le MyoPinch mesure des forces allant de 0 à 18 kg avec une résolution de 1 g et une précision de 10 g.
Fabriqué et distribué par les Ateliers Laumonier (contact@laumonier.fr).

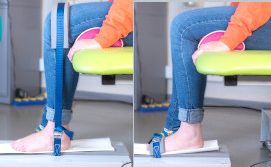 MyoAnkle – Un dynamomètre pour l’évaluation de la force de flexion et d’extension de la cheville
MyoAnkle – Un dynamomètre pour l’évaluation de la force de flexion et d’extension de la cheville
Le MyoAnkle est un dynamomètre électronique spécialement conçu pour mesurer les forces de flexion et d’extension de la cheville de manière fiable et reproductible. La gamme de mesures du MyoAnkle est adaptée aux patients atteints de pathologies musculaires ainsi qu’aux personnes saines.
Fabriqué et distribué par les Ateliers Laumonier (contact@laumonier.fr).
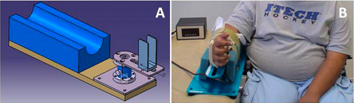 MyoWrist – Un dynamomètre pour l’évaluation de la force de flexion et d’extension du poignet
MyoWrist – Un dynamomètre pour l’évaluation de la force de flexion et d’extension du poignet
Le MyoWrist est un dynamomètre électronique spécialement conçu pour mesurer les forces de flexion et d’extension du poignet de manière fiable et reproductible. La gamme de mesures du MyoWrist est adaptée aux patients atteints de pathologies musculaires (de 0.1 Nm à 5 Nm) ainsi qu’aux personnes saines (25 Nm). L’ergonomie du dispositif est également adaptée à l’utilisation par un patient en fauteuil. Le MyoWrist est réglable, il permet donc de faire des mesures sur des enfants ou des adultes.

 MyoQuad – Un dynamomètre pour l’évaluation de la force des extenseurs du genou (breveté)
MyoQuad – Un dynamomètre pour l’évaluation de la force des extenseurs du genou (breveté)
Le MyoQuad est un dynamomètre électronique spécialement conçu pour mesurer la force des muscles extenseurs du genou et adapté aux patients très faibles. Le MyoQuad a été conçu pour être utilisé aussi bien à l’hôpital qu’à la maison ou dans une consultation de ville. L’idée est qu’il puisse s’accrocher à n’importe quel pied de lit médical, de chaise, un pied rond ou rectangulaire… Le dynamomètre, qui s’accroche d’un côté à un support fixe et de l’autre à la cheville du patient, est connecté en Bluetooth à un ordinateur, ce qui permet de visualiser en temps réel les mesures, via une application dédiée. Il est capable de détecter des variations de force de 10 g avec une précision de 50 g.
Fabriqué et distribué par les Ateliers Laumonier (contact@laumonier.fr).

 MoviPlate – Un dispositif pour l’évaluation de la motricité distale du membre supérieur (breveté)
MoviPlate – Un dispositif pour l’évaluation de la motricité distale du membre supérieur (breveté)
La MoviPlate est un instrument d’évaluation de la motricité des membres supérieurs particulièrement adapté aux patients non ambulants. Elle permet d’évaluer l’efficacité des thérapies sur la motricité distale des membres supérieurs dans le cadre des essais thérapeutiques.
Fabriqué et distribué par Valotec (contact@valotec.fr).
Protocoles et Publications dans lesquelles les MyoTools ont été utilisés
Parmi les outils développés par le Laboratoire, les dynamomètres MyoGrip et MyoPinch ont été diffusés et utilisés dans plusieurs études d’’histoire naturelle (DMD, SMA, GNE, IBM, CNM, MTM, LGMD, GSDIII) et essais thérapeutiques (Solid, Dynacure, Antisense, Généthon). Ils restent à l’heure actuelle les plus sensibles et précis sur le marché. Ils ont donné lieu à de nombreuses publications dont les plus emblématiques concernent la DMD (Servais et al, 2013; Seferian et al, 2015; Hogrel et al, 2016, 2020; Ricotti et al, 2016, 2019) et la SMA (Seferian et al, 2015; Chabanon et al, 2018; Querin et al, 2021; Annoussamy et al, 2021).
Formation MyoTools
Vous avez acquis l’un de nos dispositifs d’évaluation musculaire ? Une formation à leur utilisation par vidéoconférence ou sur place, ainsi qu’un manuel d’utilisation et une feuille de recueil de données vous sont proposés sur demande à myohelp@institut-myologie.org.
Contrôle qualité
Un contrôle qualité des données recueillies par les outils développés par le Laboratoire peut être effectué dans le cadre des protocoles de recherche clinique. L’enjeu est de pouvoir garantir la qualité des données collectées. Pour les MyoGrip, MyoPinch et Moviplate, un enregistrement des évaluations est possible à l’aide d’un logiciel dédié. Cela permet une relecture a posteriori des signaux enregistrés en cas de doute sur la fiabilité des résultats.
Données normatives-l’application MyoTools - MyoApp
Les données normatives sont obtenues à partir de données recueillies chez des enfants et des adultes en bonne santé. Des modèles prédictifs sont ensuite établis, permettant le calcul de la valeur normale attendue pour un individu en fonction de son âge, de sa taille, de son poids, de son sexe ou d’autres variables. A titre d’exemple, l’application ci-dessous permet de calculer rapidement la valeur prédite de la force mesurée avec des MyoTools.
Disclaimer
The information, including but not limited to, text, graphics, images and other material contained on this website are for informational purposes only. It is not intended to be a substitute for professional medical advice, diagnosis or treatment. Always seek the advice of your physician or other qualified health care provider with any questions you may have regarding a medical condition or treatment and before undertaking a new health care regimen, and never disregard professional medical advice or delay in seeking it because of something you have read on this website.
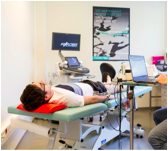 Évaluation du volume musculaire régionale par bio-impédancemétrie – ElecMyo
Évaluation du volume musculaire régionale par bio-impédancemétrie – ElecMyo
Nous développons de nouvelles approches reposant sur l’étude des propriétés électriques des tissus biologiques pour quantifier la masse musculaire régionale (par exemple la cuisse). Ces travaux impliquent le développement d’objets (ex : interface peau-électrode), de modèles in silico, et la collection de données chez des volontaires sains dans des contextes physiologiques variés (immobilisation, entrainement, …) et chez des patients souffrant de pathologies neuromusculaires ou à retentissement musculaire. Ces travaux sont réalisés en collaboration avec le laboratoire RMN de l’Institut de Myologie, le département de Neuro-Myologie, et le département de Médecine Interne de l’APHP-SU.
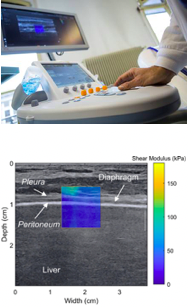 Echographie multiparamétrique des muscles locomoteurs et respiratoires – RespiMyo
Echographie multiparamétrique des muscles locomoteurs et respiratoires – RespiMyo
Nous développons de nouvelles approches reposant sur l’échographie multiparamétrique pour la caractérisation de la structure et de la fonction du muscle. Ces travaux incluent notamment l’utilisation de l’imagerie onde plane ultra-rapide, l’imagerie de déformation, et l’élastographie par l’onde de cisaillement. Au sein de cette thématique, le projet grande ambition RespiMyo se concentre sur l’application de l’échographie multiparamétrique dans le diaphragme afin de proposer des alternatives spécifiques et non invasives pour l’évaluation de la dysfonction diaphragmatique associée à des pathologies neuromusculaires, respiratoires, ou celles induite par la ventilation mécanique en soins intensifs. Ces travaux sont réalisés en collaboration avec le laboratoire RMN de l’Institut de Myologie, le laboratoire BIOMAPS (Université Paris-Sud – CEA), le département R3S (Respiration, Réanimation, Réhabilitation, Sommeil) de l’APHP-SU, et le Centre Médical Universitaire Radboud-UMC aux Pays-Bas.
Autres méthodes et dispositifs développés au NeuPEL
MyoTone Test - Évaluation de la myotonie par modélisation de la courbe de relaxation de force
Le MyoTone Test a été développé en 2008 afin d’évaluer en moins de 10 min le temps de réaction, la force volontaire maximale de préhension et la myotonie après une contraction sous-maximale à 70 % de la force volontaire maximale. La myotonie est estimée par modélisation par un logiciel supervisé.
Analyse de la marche par accélérométrie
L’analyse de la marche par accélérométrie est un outil prometteur dans l’étude des paramètres cliniques de la marche. En effet, cette technique est capable de fournir des informations utiles sur les caractéristiques (paramètres quantitatifs) de la marche chez l’homme sain ou atteint de pathologies neuromusculaires. Les enregistrements sont effectués avec un accéléromètre tri-dimensionnel qui enregistre tous les mouvements du centre de gravité au cours de la marche. Les analyses sont réalisées avec un logiciel développé au laboratoire qui permet le calcul des paramètre spatio-temporels de la marche sur les signaux accélérométriques.
Grip-Ball - Balle connectée pour la mesure et la rééducation de la force de préhension (breveté)
La Grip-Ball est un outil d’évaluation et de rééducation de la force de préhension palmaire utilisable par la personne elle-même par un simple mouvement de compression de la balle dans sa main. Elle se compose d’une balle en plastique souple, gonflable, étanche à l’air, dans laquelle sont intégrés un capteur de pression et de température, et une fonction de numérisation (Bluetooth). Les résultats peuvent être enregistrés et affichés sur le terminal local, puis transmis par la suite à un serveur. La Grip-Ball a été développée en partenariat avec l’Université de Technologie de Troyes.
ELAPS - Système de mesure d’EMG à haute résolution spatiale (breveté)
L’EMG à haute résolution spatiale, basé sur l’utilisation d’un système multi-électrodes combiné à une procédure de filtrage spatial, présente à l’heure actuelle le meilleur compromis entre la sélectivité de l’aiguille et la représentativité de l’électrode de surface classique. Le système permet la détection de l’activité d’une seule unité motrice (MU) de manière non invasive et permet la détermination de la vitesse de conduction de ces unités motrices. La distribution des vitesses de conduction est indirectement liée à la taille des fibres musculaires. En outre, l’EMG à haute résolution spatiale détecte les changements dans les activités électriques des MUs qui sont typiques de certaines pathologies neuromusculaires et neurologiques.
Évaluation de dispositifs d’assistance – AssistMyo
 Nous évaluons la sécurité, la faisabilité, et l’efficacité à court et à long terme de dispositifs d’augmentation/compensation innovants chez des patients porteurs de pathologie neuromusculaire.
Nous évaluons la sécurité, la faisabilité, et l’efficacité à court et à long terme de dispositifs d’augmentation/compensation innovants chez des patients porteurs de pathologie neuromusculaire.
Les appareils d’assistance motorisés, regroupés sous le terme exosquelettes, ont un fort potentiel pour compenser la faiblesse musculaire et ainsi améliorer la mobilité et l’indépendance des patients, et ce en dehors du cadre de la réhabilitation.
Exercice et activité physique dans les pathologies neuromusculaires – ExMyo
 Nous étudions les effets des interventions basées sur l’exercice sur la fonction neuromusculaire. Nous étudions également l’impact des troubles neuromusculaires sur l’activité physique quotidienne en fonction des pathologies et des variables cliniques. Nous utilisons des méthodes de quantification objective de l’activité physique telles que l’accélérométrie couplée à des approches innovantes en matière de traitement du signal. Nous menons également des études prospectives pour évaluer les effets d’une augmentation de l’activité physique quotidienne et/ou de programmes d’exercices structurés (force et/ou endurance) chez les patients atteints de maladies neuromusculaires.
Nous étudions les effets des interventions basées sur l’exercice sur la fonction neuromusculaire. Nous étudions également l’impact des troubles neuromusculaires sur l’activité physique quotidienne en fonction des pathologies et des variables cliniques. Nous utilisons des méthodes de quantification objective de l’activité physique telles que l’accélérométrie couplée à des approches innovantes en matière de traitement du signal. Nous menons également des études prospectives pour évaluer les effets d’une augmentation de l’activité physique quotidienne et/ou de programmes d’exercices structurés (force et/ou endurance) chez les patients atteints de maladies neuromusculaires.
Les travaux actuels sont menés en collaboration avec le Département de Neuro-Myologie et le Département de Médecine Interne de l’APHP-SU. Les membres du laboratoire sont également largement impliqués dans l’élaboration des recommandations concernant l’activité physique et l’exercice dans les maladies neuromusculaires (MEDICOSPORT Santé).
Activités de diagnostic clinique
Grip Test -Test d’exercice non ischémique de l’avant-bras pour le dépistage de patients présentant une intolérance à l’effort
Le Grip Test est un test utilisé pour l’aide au diagnostic des pathologies musculaires métaboliques. Il consiste à évaluer la force de préhension maximale et à faire effectuer au patient un travail musculaire standardisé. Des prélèvements sanguins réguliers permettent l’analyse de plusieurs métabolites (notamment lactate et ammoniémie) dont la concentration sanguine doit changer du fait de l’effort effectué. L’analyse de l‘évolution des concentrations permet ainsi d’orienter le diagnostic.
Le Grip Test a été inventé en 1998 et mis en place en 2000 dans le service de Neuro-Myologie en remplacement du test dit “du garrot”, potentiellement douloureux, voire dangereux. Depuis, près de 2000 patients en ont bénéficié pour l’orientation de leur diagnostic. Plusieurs algorithmes diagnostiques ont été proposés pour la détection des glycogénoses et des dystrophies pseudo-métaboliques. Ainsi, le Grip Test permet la détection de la glycogénose 5 (GSD5, maladie de McArdle) avec une sensibilité de 100 % et une spécificité de 99.7 % (Hogrel et al, 2015). L’hyperammoniémie est un critère fort en faveur d’un diagnostic de glycogénose (Hogrel et al, 2017) puisque, outre la GSD5, elle peut orienter vers un diagnostic d’autres glycogénoses (déficit en enzyme débranchant (AGL), phosphorylase-b kinase (PHKA1), phosphoglycerate kinase 1 (PGK1), phosphoglucomutase-1 (PGM1)). L’’analyse des CPK 24H après le test est également informative. Un Grip Test normal accompagné d’une augmentation significative de CPK à 24H (+300 UI/L) suggère une dystrophie pseudo-métabolique (principalement LGMD ou Becker). Ces travaux sont réalisés en collaboration avec le service de Neuro-Myologie APHP-SU.
Implication dans la recherche clinique
 En collaboration étroite avec le département des essais clinique I-Motion Adultes, nous sommes impliqués dans de nombreuses études cliniques (histoires naturelles et essais thérapeutiques) en tant que promoteur ou centre investigateur pour des promoteurs externes, y compris des start-up et des petites et grandes sociétés pharmaceutiques.
En collaboration étroite avec le département des essais clinique I-Motion Adultes, nous sommes impliqués dans de nombreuses études cliniques (histoires naturelles et essais thérapeutiques) en tant que promoteur ou centre investigateur pour des promoteurs externes, y compris des start-up et des petites et grandes sociétés pharmaceutiques.
Expertise et services
Activités de conseil
Le NeuPel exerce des activités de conseil auprès d’universitaires et d’industriels telles que la conception et le suivi d’études (moyens d’évaluation, outcomes, …).
Equipements et techniques disponibles
- Electromyographie filaire (Digitimer) et sans fil (Delsys)
- Capture et analyse du mouvement par centrales inertielles (Opale, APDM)
- Dynamomètre isocinétique (Biodex)
- Dynamométrie manuelle et stabilisée (MicroFet, Lafayette, QMT, dispositifs développés en interne)
- Dépense métabolique-analyse des gaz respiratoires
- Spirométrie et exploration de la force des muscles respiratoires
- Stimulation électrique (Digitimer)
- Stimulation magnétique (Magstim, bobine donut/8, bistim)
- Echographe x 2 (Aixplorer, Supersonic Imagine)
- Evaluation de l’activité physique quotidienne (Geneactiv, Actigraph; AX3, Axivity)
- Plateforme de force (AMTI)
- Rameur x 3
Brevets
Les approches innovantes développées par le NeuPel mènent régulièrement à des dépôts de brevets. A ce jour, une douzaine d’innovations ont déjà été brevetées.
Nos dernières publications
- Birnbaum, S., Sharshar, T., & Hogrel, J.-Y. (2023). Exercise Training for autoimmune myasthenia gravis: A review of safety and effectiveness based on existing literature . RRNMF Neuromuscular Journal, 4(3). https://doi.org/10.17161/rrnmf.v4i3.18699
- Sharshar, T., Mazeraud, A., & Birnbaum, S. (2023). Corticosteroids in Generalized Autoimmune Myasthenia Gravis: A Narrative Review. RRNMF Neuromuscular Journal, 4(3). https://doi.org/10.17161/rrnmf.v4i3.19542
- Birnbaum S, Sharshar T, Ropers J, Portero P, Hogrel J. Neuromuscular fatigue in autoimmune myasthenia gravis: a cross-sectional study. Neurophysiol Clin. 2023;53(4).
- Poulard T, Bachasson D, Fossé Q, Niérat MC, Hogrel JY, Demoule A, Gennisson JL, Dres M. Poor correlation between diaphragm thickening fraction and transdiaphragmatic pressure in Mechanically Ventilated Patients and Healthy Subjects. Anesthesiology. 2021 Nov 16. doi: 10.1097/ALN.0000000000004042.
- Trucco F, Ridout D, Domingos J, Maresh K, Chesshyre M, Munot P, Sarkozy A, Robb S, Quinlivan R, Riley M, Wallis C, Chan E, Abel F, De Lucia S, Hogrel JY, Niks EH, de Groot I, Servais L, Straub V, Ricotti V, Manzur A, Muntoni F; UK NorthStar Clinical Network and AFM Network. Genotype-related respiratory progression in Duchenne Muscular Dystrophy – multicentre international study. Muscle Nerve. 2021 Oct 4. doi: 10.1002/mus.27427.
- Pini J, Siciliano G, Lahaut P, Braun S, Segovia-Kueny S, Kole A, Hérnando I, Selb J, Schirinzi E, Duong T, Hogrel JY, Olmedo JJS, Vissing J, Servais L, Vincent-Genod D, Vuillerot C, Bannwarth S, Eggenspieler D, Vicart S, Diaz-Manera J; eNMD group, Lochmüller H, Sacconi S. E-Health & Innovation to Overcome Barriers in Neuromuscular Diseases. Report from the 1st eNMD Congress: Nice, France, March 22-23, 2019. J Neuromuscul Dis, 8(4):742-754, 2021.
- Vignier N, Chatzifrangkeskou M, Pinton L, Wioland H, Marais T, Lemaitre M, Le Dour C, Peccate C, Cardoso D, Schmitt A, Wu W, Biferi MG, Naouar N, Macquart C, Beuvin M, Decostre V, Bonne G, Romet-Lemonne G, Worman HJ, Tedesco FS, Jégou A, Muchir A. The non-muscle ADF/cofilin-1 controls sarcomeric actin filament integrity and force production in striated muscle laminopathies. Cell Rep. 2021 Aug 24;36(8):109601. doi: 10.1016/j.celrep.2021.109601.
- Guinot M, Maindet C, Hodaj H, Hodaj E, Bachasson D, Baillieul S, Cracowski JL, Launois S. Effects of Repetitive Transcranial Magnetic Stimulation and Multicomponent Therapy in Patients With Fibromyalgia: A Randomized Controlled Trial. Arthritis Care Res (Hoboken). 2021 Mar;73(3):449-458. doi: 10.1002/acr.24118
- Benveniste O, Hogrel JY, Belin L, Annoussamy M, Bachasson D, Rigolet A, Laforet P, Dzangué-Tchoupou G, Salem JE, Nguyen LS, Stojkovic T, Zahr N, Hervier B, Landon-Cardinal O, Behin A, Guilloux E, Reyngoudt H, Amelin D, Uruha A, Mariampillai K, Marty B, Eymard B, Hulot JS, Greenberg SA, Carlier PG, Allenbach Y. Sirolimus for treatment of patients with inclusion body myositis: a randomised, double-blind, placebo-controlled, proof-of-concept, phase 2b trial. Lancet Rheum, 3(1):E40-E48, 2021.
- Amato AA, Hanna MG, Machado PM, Badrising UA, Chinoy H, Benveniste O, Karanam AK, Wu M, Tankó LB, Schubert-Tennigkeit AA, Papanicolaou DA, Lloyd TE, Needham M, Liang C, Reardon KA, de Visser M, Ascherman DP, Barohn RJ, Dimachkie MM, Miller JAL, Kissel JT, Oskarsson B, Joyce NC, Van den Bergh P, Baets J, De Bleecker JL, Karam C, David WS, Mirabella M, Nations SP, Jung HH, Pegoraro E, Maggi L, Rodolico C, Filosto M, Shaibani AI, Sivakumar K, Goyal NA, Mori-Yoshimura M, Yamashita S, Suzuki N, Aoki M, Katsuno M, Morihata H, Murata K, Nodera H, Nishino I, Romano CD, Williams VSL, Vissing J, Zhang Auberson L; RESILIENT Study Extension Group. Efficacy and Safety of Bimagrumab in Sporadic Inclusion Body Myositis: Long-term Extension of RESILIENT. Neurology. 2021 Mar 23;96(12):e1595-e1607. doi: 10.1212/WNL.0000000000011626. Epub 2021 Feb 17. PMID: 33597289; PMCID: PMC8032371.
- Home-based exercise in autoimmune myasthenia gravis: A randomized controlled trial. Birnbaum S, Porcher R, Portero P, Clair B, Demeret S, Eymard B, Gargiulo M, Louët E, Berrih-Aknin S, Le Panse R, Aegerter P, Hogrel JY, Sharshar T; MGEX Study Group. Neuromuscul Disord. 2021 Aug;31(8):726-735. doi: 10.1016/j.nmd.2021.05.002. Epub 2021 May 27. PMID: 34304969.
- Upper limb disease evolution in exon 53 skipping eligible patients with Duchenne muscular dystrophy. Lilien C, Reyngoudt H, Seferian AM, Gidaro T, Annoussamy M, Chê V, Decostre V, Ledoux I, Le Louër J, Guemas E, Muntoni F, Hogrel JY, Carlier PG, Servais L; PreU7 Study Group. . Ann Clin Transl Neurol. 2021 Oct;8(10):1938-1950. doi: 10.1002/acn3.51417. Epub 2021 Aug 28. PMID: 34453498; PMCID: PMC8528463.
- Adequate Initial Dosage and Tapering Methods of Steroids to Reduce the Total Corticosteroid Dose in Myasthenia Gravis-Reply. Birnbaum S, Porcher R, Sharshar T. JAMA Neurol. 2021 Sep 1;78(9):1153-1154. doi: 10.1001/jamaneurol.2021.2495. PMID: 34338728.
- MRI and muscle imaging for idiopathic inflammatory myopathies. Malartre S, Bachasson D, Mercy G, Sarkis E, Anquetil C, Benveniste O, Allenbach Y. Brain Pathol. 2021 May;31(3):e12954. doi: 10.1111/bpa.12954. PMID: 34043260; PMCID: PMC8412099.
- North Star Ambulatory Assessment changes in ambulant Duchenne boys amenable to skip exons 44, 45, 51, and 53: A 3 year follow up. Coratti G, Pane M, Brogna C, Ricotti V, Messina S, D’Amico A, Bruno C, Vita G, Berardinelli A, Mazzone E, Magri F, Ricci F, Mongini T, Battini R, Bello L, Pegoraro E, Baranello G, Previtali SC, Politano L, Comi GP, Sansone VA, Donati A, Hogrel JY, Straub V, De Lucia S, Niks E, Servais L, De Groot I, Chesshyre M, Bertini E, Goemans N, Muntoni F, Mercuri E; on behalf on the International DMD Group and the iMDEX Consortium. PLoS One. 2021 Jun 25;16(6):e0253882. doi: 10.1371/journal.pone.0253882. PMID: 34170974; PMCID: PMC8232423.
- A novel PHKA1 mutation associating myopathy and cognitive impairment: Expanding the spectrum of phosphorylase kinase b (PhK) deficiency. Bisciglia M, Froissart R, Bedat-Millet AL, Romero NB, Pettazzoni M, Hogrel JY, Petit FM, Stojkovic T. J Neurol Sci. 2021 May 15;424:117391. doi: 10.1016/j.jns.2021.117391. Epub 2021 Mar 18. PMID: 33799212.
- Free-Living Physical Activity and Sedentary Behaviour in Autoimmune Myasthenia Gravis: A Cross-Sectional Study. Birnbaum S, Bachasson D, Sharshar T, Porcher R, Hogrel JY, Portero P. J Neuromuscul Dis. 2021;8(4):689-697. doi: 10.3233/JND-210637. PMID: 33843693.
- Still seeking the holy grail of outcome measures in inclusion body myositis. Hogrel JY. J Neurol Neurosurg Psychiatry. 2021 Apr 13:jnnp-2021-326460. doi: 10.1136/jnnp-2021-326460. Epub ahead of print. PMID: 33849998.
- Reply to ‘Letter to the editor: is maximal diaphragm tissue velocity suited for the assessment of diaphragm contractility?’ Poulard T, Dres M, Niérat MC, Rivals I, Hogrel JY, Similowski T, Gennisson JL, Bachasson D. J Physiol. 2021 Apr;599(8):2343-2344. doi: 10.1113/JP281433. Epub 2021 Mar 18. PMID: 33660853.
- Assessing Dysferlinopathy Patients Over Three Years With a New Motor Scale. Jacobs MB, James MK, Lowes LP, Alfano LN, Eagle M, Muni Lofra R, Moore U, Feng J, Rufibach LE, Rose K, Duong T, Bello L, Pedrosa-Hernández I, Holsten S, Sakamoto C, Canal A, Sanchez-Aguilera Práxedes N, Thiele S, Siener C, Vandevelde B, DeWolf B, Maron E, Guglieri M, Hogrel JY, Blamire AM, Carlier PG, Spuler S, Day JW, Jones KJ, Bharucha-Goebel DX, Salort-Campana E, Pestronk A, Walter MC, Paradas C, Stojkovic T, Mori-Yoshimura M, Bravver E, Díaz-Manera J, Pegoraro E, Mendell JR; Jain COS Consortium, Mayhew AG, Straub V. Ann Neurol. 2021 May;89(5):967-978. doi: 10.1002/ana.26044. Epub 2021 Feb 26. PMID: 33576057.
- Lean regional muscle volume estimates using explanatory bioelectrical models in healthy subjects and patients with muscle wasting. Bachasson D, Ayaz AC, Mosso J, Canal A, Boisserie JM, Araujo ECA, Benveniste O, Reyngoudt H, Marty B, Carlier PG, Hogrel JY.J Cachexia Sarcopenia Muscle. 2021 Feb;12(1):39-51. doi: 10.1002/jcsm.12656. Epub 2020 Dec 29. PMID: 33377299; PMCID: PMC7890267.
- Natural history of Type 2 and 3 spinal muscular atrophy: 2-year NatHis-SMA study. Annoussamy M, Seferian AM, Daron A, Péréon Y, Cances C, Vuillerot C, De Waele L, Laugel V, Schara U, Gidaro T, Lilien C, Hogrel JY, Carlier P, Fournier E, Lowes L, Gorni K, Ly-Le Moal M, Hellbach N, Seabrook T, Czech C, Hermosilla R, Servais L; NatHis-SMA study group. Ann Clin Transl Neurol. 2021 Feb;8(2):359-373. doi: 10.1002/acn3.51281. Epub 2020 Dec 24.
- Comparison of Corticosteroid Tapering Regimens in Myasthenia Gravis: A Randomized Clinical Trial. Sharshar T, Porcher R, Demeret S, Tranchant C, Gueguen A, Eymard B, Nadaj-Pakleza A, Spinazzi M, Grimaldi L, Birnbaum S, Friedman D, Clair B; MYACOR Study Group. JAMA Neurol. 2021 Apr 1;78(4):426-433. doi: 10.1001/jamaneurol.2020.5407. PMID: 33555314; PMCID: PMC7871208.
- Non-invasive assessment of skeletal muscle fibrosis in mice using nuclear magnetic resonance imaging and ultrasound shear wave elastography. Martins-Bach AB, Bachasson D, Araujo ECA, Soustelle L, Loureiro de Sousa P, Fromes Y, Carlier PG. Sci Rep. 2021 Jan 11;11(1):284. doi: 10.1038/s41598-020-78747-8. PMID: 33431931; PMCID: PMC7801669.
- Hierarchical Bayesian modelling of disease progression to inform clinical trial design in centronuclear myopathy. Fouarge E, Monseur A, Boulanger B, Annoussamy M, Seferian AM, De Lucia S, Lilien C, Thielemans L, Paradis K, Cowling BS, Freitag C, Carlin BP, Servais L; NatHis-MTM Study Group. Orphanet J Rare Dis. 2021 Jan 6;16(1):3. doi: 10.1186/s13023-020-01663-7. PMID: 33407688; PMCID: PMC7789189.
- Development of new outcome measures for adult SMA type III and IV: a multimodal longitudinal study. Querin G, Lenglet T, Debs R, Stojkovic T, Behin A, Salachas F, Le Forestier N, Amador MDM, Bruneteau G, Laforêt P, Blancho S, Marchand-Pauvert V, Bede P, Hogrel JY, Pradat PF. J Neurol. 2021 May;268(5):1792-1802. doi: 10.1007/s00415-020-10332-5. Epub 2021 Jan 2. PMID: 33388927.
- Routine monitoring of isometric knee extension strength in patients with muscle impairments using a new portable device: cross-validation against a standard isokinetic dynamometer. Hogrel JY, Benveniste O, Bachasson D. Physiol Meas. 2020;41(1):015003. Published 2020 Feb 5. doi:10.1088/1361-6579/ab6b49
- Normalized grip strength is a sensitive outcome measure through all stages of Duchenne muscular dystrophy, Hogrel JY, Decostre V, Ledoux I, de Antonio M, Niks E H, de Groot I, Straub V, Muntoni F, Ricotti V, Voit T, Seferian A, Gidaro T & Servais L. [published online ahead of print, 2020 Mar 21]. J Neurol. 2020;10.1007/s00415-020-09800-9. doi:10.1007/s00415-020-09800-9
- Determinants of Performance in the Timed Up-and-Go and Six-Minute Walk Tests in Young and Old Healthy Adults. Montgomery G, McPhee J, Pääsuke M, Sipilä S, Maier A B, Hogrel JY, Degens H. J Clin Med. 2020;9(5):1561. Published 2020 May 21. doi:10.3390/jcm9051561
- An embryonic CaVβ1 isoform promotes muscle mass maintenance via GDF5 signaling in adult mouse. Traoré M, Gentil C, Benedetto C, Hogrel JY, De la Grange P, Cadot B, Benkhelifa-Ziyyat S, Julien L, Lemaitre M, Ferry A, Piétri-Rouxel F, Falcone S. Sci Trans Med, 11(517):eaaw1131, 2019.
- Scapular dyskinesis in myotonic dystrophy type 1: clinical characteristics and genetic investigations. Voermans NC, van der Bilt RC, IJspeert J, Hogrel JY, Jeanpierre M, Behin A, Laforet P, Stojkovic T, van Engelen BG, Padberg GW, Sacconi S, Lemmers RJLF, van der Maarel SM, Eymard B, Bassez G. J Neurol. 2019 Dec;266(12):2987-2996.
- Whole-body muscle magnetic resonance imaging in glycogen-storage disease type III. Tobaly D, Laforêt P, Perry A, Habes D, Labrune P, Decostre V, Masingue M, Petit F, Barp A, Bello L, Carlier P, Carlier RY. Muscle Nerve, 2019 Jul;60(1):72-79.
- Large variation in effects during 10-years of enzyme-therapy in adults with Pompe disease. Harlaar L, Hogrel JY, Perniconi BP, Kruijshaar ME, Rizopoulos D, Taouagh N, Canal A, Brusse E, van Doorn PA, van der Ploeg AT, Laforêt P, van der Beek NAME. Neurology 2019 Nov 5;93(19):e1756-e1767.
- ENMC workshop study group. 237th ENMC International Workshop: GNE myopathy – current and future research Hoofddorp, The Netherlands, 14-16 September 2018. Pogoryelova O, Urtizberea JA, Argov Z, Nishino I, Lochmüller H, Neuromuscul Disord. 29:401-410, 2019.
- Hyperammonaemia following exercise may also reveal PGK1 deficiency. Hogrel JY, Ledoux I, Béhin A. J Clin Pathol, 72(6):452, 2019.
- Respiratory and upper limb outcome measures in ambulant and non-ambulant subjects with Duchenne muscular dystrophy: a prospective multicentre study. Ricotti V, Selby V, Ridout D, Domingos J, Decostre V, Mayhew A, Eagle M, Butler J, Guglieri M, Van der Holst M, Jansen M, Verschuuren JJGM, de Groot I, Niks E, Servais L, Straub V, Voit T, Hogrel JY, Muntoni F. Neuromuscul Dis, 29(4):261-268, 2019.
- Diaphragm shear modulus reflects transdiaphragmatic pressure during isovolumetric inspiratory efforts and ventilation against inspiratory loading. Bachasson D, Dres M, Niérat MC, Gennisson JL, Hogrel JY, Doorduin J, Similowski T. J App Physiol, 126(3):699-707, 2019.
- X-linked Myotubular Myopathy: A prospective international natural history study. Annoussamy M, Lilien C, Gidaro T, Gargaun E, Chê V, Schara U, Gangfuß A, D’Amico A, Dowling JJ, Darras BT, Daron A, Hernandez A, de Lattre C, Arnal JM, Mayer M, Cuisset JM, Vuillerot C, Fontaine S, Bellance R, Biancalana V, Buj-Bello A, Hogrel JY, Landy H, Servais L. Neurology, 92:e1852-e1867, 2019.
- Association of interleukin-6 rs1800796 polymorphism with reduced cognitive performance in healthy older adults. Bezuch NE, Bradburn S, Sipilä S, Pääsuke M, Gapeyeva H, Maier AB, Hogrel JY, Barnouin Y, Butler-Browne G, Narici M, McPhee J, Murgatroyd C. Meta Gene, 19:51-55, 2019.
- Assessment of disease progression in dysferlinopathy – a one year cohort study. Moore U, Jacobs M, James MK, Mayhew AG, Fernandez-Torron R, Feng J, Cnaan A, Eagle M, Bettinson K, Rufibach LE, Muni Lofra R, Blamire AM, Carlier PG, Mittal P, Pax Lowes L, Alfano L, Rose K, Duong T, Berry KM, Montiel-Morillo E, Pedrosa-Hernández I, Holsten S, Sanjak M, Ashida A, Sakamoto C, Tateishi T, Yajima H, Canal A, Ollivier G, Decostre V, Bosco Mendez J, Sánchez-Aguilera Praxedes N, Thiele S, Siener C, Shierbecker J, Florence JM, Vandevelde B, DeWolf B, Hutchence M, Gee R, Prugel J, Maron E, Hilsden H, Lochmüller H, Grieben U, Spuler S, Tesi Rocha C, Day JW, Jones KJ, Bharucha-Goebel DX, Salort-Campana E , Harms M, Pestronk A, Krause S, Schreiber-Katz O, Walter MC, Paradas C, Hogrel JY, Stojkovic T, Takeda S, Mori-Yoshimura M, Bravver E, Sparks S, Díaz-Manera J, Bello L, Semplicini C, Pegoraro E, Mendell JR, Bushby K, Straub V, for the Jain COS Consortium. Neurology, 92:e461-e474, 2019.
- The clinical and radiological landscape of adult spinal-muscular atrophy: a combined spinal and cerebral neuroimaging study. Querin G, El Mendili MM, Lenglet T, Behin A, Stojkovic T, Salachas F, Le Forestier N, del Mar Amador M, Debs R, Meininger V, Bruneteau G, Lehéricy S, Laforêt P, Blancho S, Benali H, Catala M, Marchand-Pauvert V, Hogrel JY, Bede P, Pradat PF. Neuroimage Clin, 21:101618, 2019.

